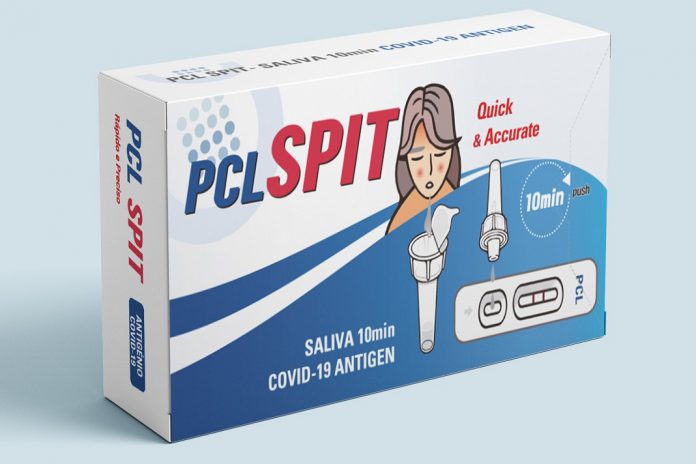
De uma forma mais simples e sem o desconforto associado aos convencionais testes de antigénio que utilizam as zaragatoas para recolha de amostra, o novo sistema de diagnóstico que vai ser lançado pela BioJam permite detetar, em apenas 15 minutos e de uma forma não invasiva, possíveis casos positivos de COVID-19.
Carlos Monteiro, CEO e fundador da farmacêutica BioJam, referiu: “A realização dos convencionais testes de antigénio, apesar de constituírem um processo rápido, não deixam de ser mais desconfortáveis, sobretudo para crianças, adolescentes e até adultos com sensibilidade ao método da zaragatoa. Com os novos testes de saliva conseguimos eliminar o desconforto mantendo a segurança dos testes que apresentam uma especificidade de 100% e uma sensibilidade de mais de 94%”.
Os testes vão estar disponíveis em Kits individuais, podendo desta forma serem adquiridos em unidades isoladas, não obrigando à aquisição de caixas de 20 testes que por vezes podem não ser necessárias. O teste rápido PCL COVID19 Ag Gold saliva é um dispositivo médico de diagnóstico in vitro que se baseia no Teste imunocromatográfico (ICA) para a deteção qualitativa do antigénio SARS-CoV-2 na saliva humana.
Mesmo não sendo um teste invasivo, este só estará disponível para realização em clínicas e laboratórios de análises clínicas devidamente registadas na ERS. O teste é realizado por profissionais de saúde ou sob o acompanhamento destes. A BioJam espera que o teste possa vir a ser distribuído pelas farmácias comunitárias.
Os testes rápidos de antigénio a partir de amostra de saliva da BioJam vão integrar a lista de testes de antigénio do INFARMED, DGS e INSA, uma vez que em Portugal, apenas são permitidos testes que apresentem os padrões de desempenho com valores de sensibilidade superior ou igual a 90% e de especificidade igual ou superior a 97%.
A farmacêutica Ibérica BioJam foi uma das primeiras empresas a disponibilizar os testes de antigénio no mercado português. A farmacêutica referiu que continua a investir na investigação das melhores soluções de diagnóstico COVID-19.
“No início de setembro, em conformidade com a legislação para Dispositivos Médicos de Diagnóstico In Vitro, notificámos o INFARMED para a distribuição dos testes rápidos antigénio NADAL COVID-19 Ag, os quais viriam a integrar a lista inicial de testes indicados pelas entidades regulamentares de saúde pública em Portugal”, referiu Carlos Monteiro.
O CEO acrescentou: “Recentemente, no início de novembro, lançámos no mercado um único dispositivo médico para diagnóstico de COVID-19 e Gripe. Hoje preparamo-nos para lançar um teste que irá permitir um diagnóstico menos invasivo e mais acessível a todos aqueles para quem o processo acaba por ser extremamente incómodo e até difícil de concretizar, reitero que há crianças, adolescentes e adultos que não propõem testar pelo desconforto da zaragatoa. Tal como a Organização Mundial da Saúde, continuamos a acreditar que testar a população em massa é uma das melhores estratégias para refrear a propagação da COVID-19”.