O Centro de Controle Estatal de Medicamentos, Equipamentos e Dispositivos Médicos (CECMED) aprovou o início de ensaios clínicos das vacinas candidatas contra COVID-19, Mambisa e Abdala após exaustiva revisão do processo que caracterizava cada uma delas, anunciou a empresa de Biotecnologia e Indústrias Farmacêutica BioCubaFarma.
A BioCubaFarma referiu, em comunicado, que o estudo da estabilidade das moléculas, a apresentação dos testes efetuados em animais e os protocolos clínicos a utilizar foram alguns dos elementos que convenceram o CECMED de que era viável apostar também nestas duas novas variantes produzidas pelo Centro de Engenharia Genética e Biotecnologia (CIGB).
Na fase I de ensaio clinico vão participar cerca de 88 indivíduos. O ensaio compreende dois esquemas de três tomas: um com ciclo curto: em que a segunda inserção é aos 14 dias após a primeira e a terceira aos 28 dias, e um longo: onde o segundo é implantado 28 dias após o primeiro e o terceiro aos 56 dias.
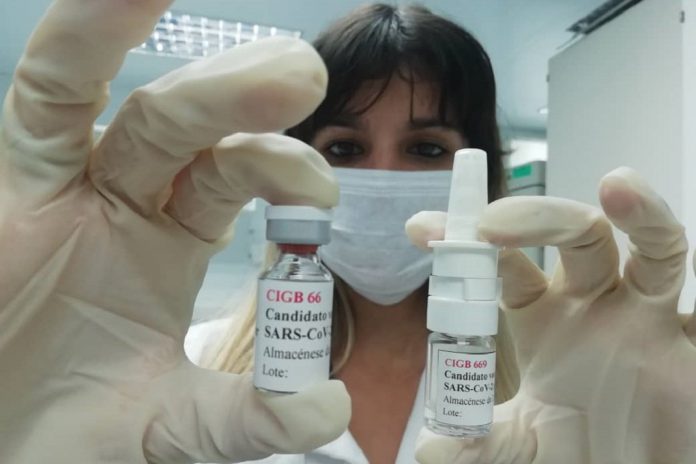
O ensaio Mambisa vai ser realizado em Havana, onde vários grupos vão receber duas formulações: uma via intramuscular e uma via nasal. O ensaio Abdala é realizado em Santiago de Cuba e apenas a versão intramuscular é testada.
Os ensaios de fase I vão permitir avaliar se há alguma reação adversa ou evento que possa causar indícios sobre a insegurança das pessoas vacinados.
Para a BioCubaFarma, apesar do caminho que ainda falta percorrer, não há dúvidas de que a confirmação de quatro vacinas candidatas na fase experimental constitui uma façanha da biotecnologia cubana e da indústria farmacêutica.