Uma nova combinação de medicamentos matou com sucesso células mamárias portadoras de mutações duplas no gene HER2. Estas células tornaram-se resistentes à terapia normalmente usada contra o cancro. O estudo foi liderado por investigadores do UT Southwestern Medical Center, EUA, e as descobertas, foram publicadas na “Cancer Research”, uma revista da Associação Americana para a Investigação do Cancro.
As descobertas podem levar a novas formas de tratar pacientes com mutações no gene HER2, que ocorrem em 5% a 7% dos cancros da mama metastáticos.
“Acreditamos que a combinação de medicamentos que exploramos pode ser uma estratégia clínica promissora para superar a resistência aos inibidores de HER2 para o subconjunto de pacientes que apresentam mutações duplas de HER2 ”, referiu Ariella B. Hanker, da UT Southwestern. A investigadora coliderou o estudo com Arnaldo Marín, da Universidade do Chile, em que a dissertação da tese teve a orientação Ariella B. Hanker.
O gene HER2, que codifica um recetor do fator de crescimento que se encontra na superfície das células mamárias, atraiu a atenção no final da década de 1980 pelo seu papel no cancro da mama e em vários outros tipos de cancro, quando foi demonstrado que as células que abrigam cópias adicionais deste gene – e, portanto, expressam mais recetores na sua superfície – sofrem um crescimento incontrolável.
Os tumores HER2 positivos representam cerca de 20% dos diagnósticos de cancro da mama. Mais recentemente, os investigadores descobriram que um subconjunto menor de tumores de cancro da mama abriga mutações HER2 promotoras de cancro que levam à atividade excessiva do recetor.
Embora estes tumores respondam inicialmente aos medicamentos inibidores do HER2, estudos demonstraram que eventualmente param de responder após o desenvolvimento de novas mutações. Embora várias dessas mutações secundárias no HER2 tenham sido identificadas, não se sabe como elas induzem resistência aos medicamentos e como superar essa resistência.
Para responder a estas questões a equipa de investigadores alterou geneticamente células mamárias saudáveis para transportar uma de duas mutações HER2 diferentes – conhecidas como HER2 L869R e HER2 L755S – devido à sua propensão para ocorrer em conjunto com mutações secundárias HER2.
Os investigadores criaram três linhagens de células mamárias com qualquer uma das duas mutações HER2, em combinação com diferentes mutações secundárias. Embora as células com mutações únicas permanecessem sensíveis ao neratinib, um medicamento normalmente prescrito para tratar tumores HER2 positivos, as células com mutações duplas eram todas resistentes ao neratinib.
Para entender como ocorreu a resistência, os investigadores da UT Southwestern em conjunto com investigadores da Vanderbilt University realizaram modelagem computacional das proteínas recetoras produzidas pelas células mutantes. Os resultados mostraram que em células com dupla mutação, a proteína HER2 resultante era ainda mais ativa do que em células nas quais o HER2 tinha uma única mutação ou nenhuma mutação. Isso permitiu que a proteína HER2 com dupla mutação lançasse sinais moleculares com mais eficiência que ajudaram as células a sobreviver e dividir-se. Além disso, as mutações duplas bloquearam parcialmente a ligação do neratinib ao HER2 para inibi-lo.
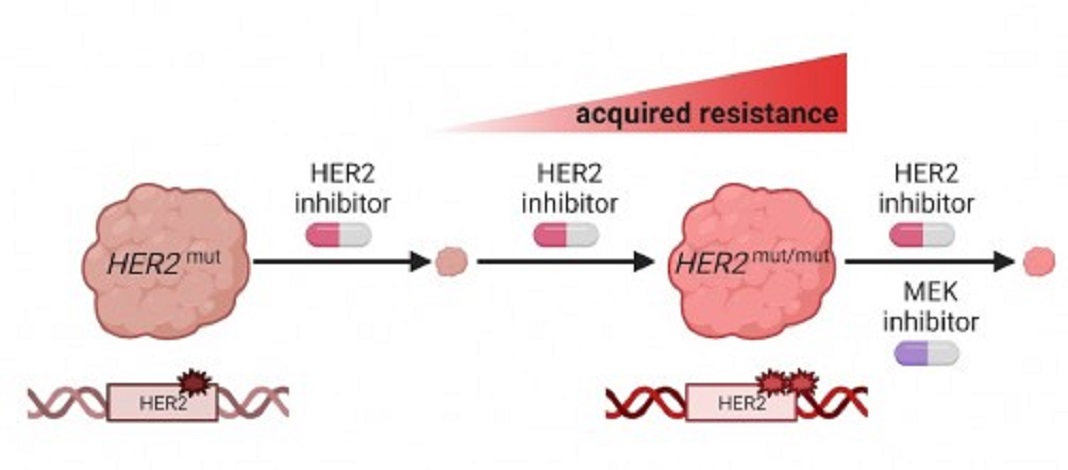
Experiencias adicionais revelaram que as proteínas HER2 com dupla mutação resistiram não apenas ao neratinib, mas também à maioria de outros medicamentos de mesma classe. No entanto, quando os investigadores trataram células portadoras de mutações duplas com inibidores MEK, que bloqueiam uma das vias de sinalização ativadas quando o recetor do fator de crescimento HER2 está ativo, a divisão abrandou e algumas células morreram. Este efeito foi amplificado quando os inibidores da MEK foram combinados com o neratinib.
Ariella B. Hanker referiu que os resultados sugerem que administrar aos pacientes um inibidor de MEK com um inibidor de HER2 poderá superar a resistência aos medicamentos inibidores de HER2 que normalmente se desenvolve com mutações duplas.
“Ambas as classes de medicamentos estão aprovadas pela FDA e provaram serem seguras e toleradas pelos pacientes. Os nossos resultados sugerem que vale a pena testar o uso em conjunto para superar a resistência ao inibidor de HER2 em ensaios clínicos”, acrescentou a investigadora.
















